Pour faire suite à l’essai de Phase I First-in-Human avec l’anti-Netrine1 (NP137) en agent unique, et envisager de proposer une thérapie innovante à des patientes atteintes de tumeurs gynécologiques agressives dont les options thérapeutiques sont limitées, un nouvel essai clinique a été mis en place, l’essai GyNET, qui est au cœur du projet DEGYN.
Mise en place de l’essai
Cet essai est porté par le Centre Léon Bérard et coordonné par la Cellule Promotion / Equipe Essais Précoces de la DRCI du CLB (Direction de la Recherche Clinique et de de l’Innovation). La Recherche clinique et de l’innovation du Centre Léon Bérard est dirigée par le Dr David Pérol. Son objectif dans les années à venir est de poursuivre l’évaluation de nouvelles thérapeutiques, notamment par la réalisation d’essais cliniques centrés sur l’identification d’altérations moléculaires. Ces études permettant d’envisager l’adaptation des traitements en fonction des anomalies génétiques détectées dans les tumeurs, ce que l’on dénomme aujourd’hui communément : médecine de précision.
L’activité de recherche clinique est composée de 4 pôles de compétences: Promotion, Investigation, Biostatistiques, Innovations et Stratégies et 2 fonctions support (Data Management et Affaires réglementaires et Qualité).
Le Centre Léon Bérard compte plus de 350 essais ouverts aux inclusions avec 17,2% des patients pris en charge inclus dans des essais cliniques, un gage d’innovation pour la prise en charge des patients.
L’essai clinique GyNET
GyNET est un essai de Phase I/II, coordonné par le Pr Isabelle Ray-Coquard, MD, PhD:
GYNecological Cancers Treated With NETrin mAbs in Combination With Chemotherapy and /or Pembrolizumab (GYNET) (NCT04652076)
Il est destinée aux patientes atteintes d’un cancer avancé/métastatique du col de l’utérus ou de l’endomètre.
L’essai de Phase I, First-in-Human a montré des résultats prometteurs sur des tumeurs gynécologiques, en agent unique. Afin d’augmenter les chances de réponses, et au vu de l’agressivité des tumeurs ciblées, le design de l’essai GyNET propose d’évaluer l’impact du NP137 en combinaison avec des thérapies conventionnelles et/ou de l’immunothérapie. La société MSD France fournit gracieusement un anti-PDL1, le Pembrolizumab pour la réalisation de l’étude clinique..
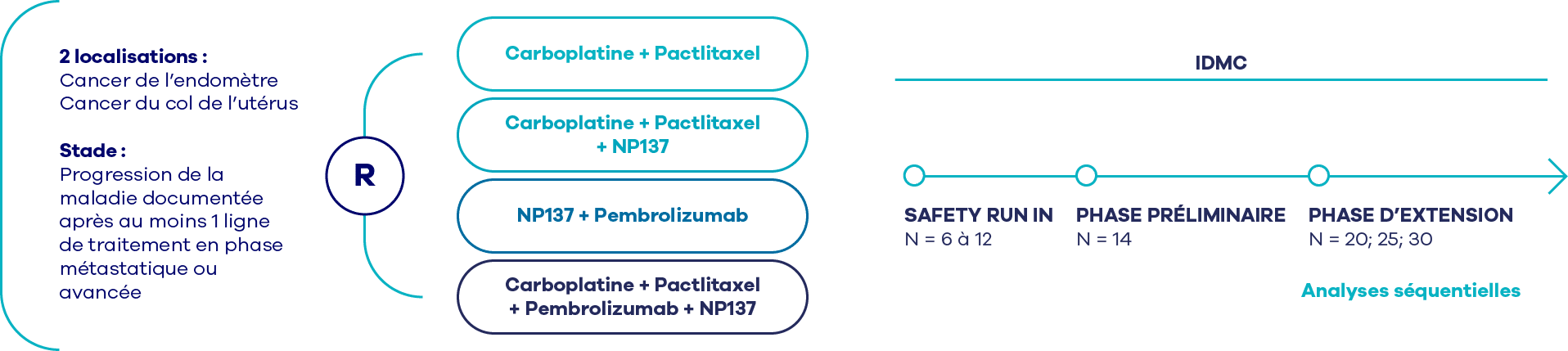
L’essai clinique est conçu de telle sorte que la (ou les) combinaison d’intérêt présentant un bénéfice clinique via des analyses intermédiaires fréquentes (approche Bayésienne) du taux de réponse objective à 3 mois selon RECIST V1.1 sera(ont) sélectionnées rapidement, pour le bénéfice des patientes.
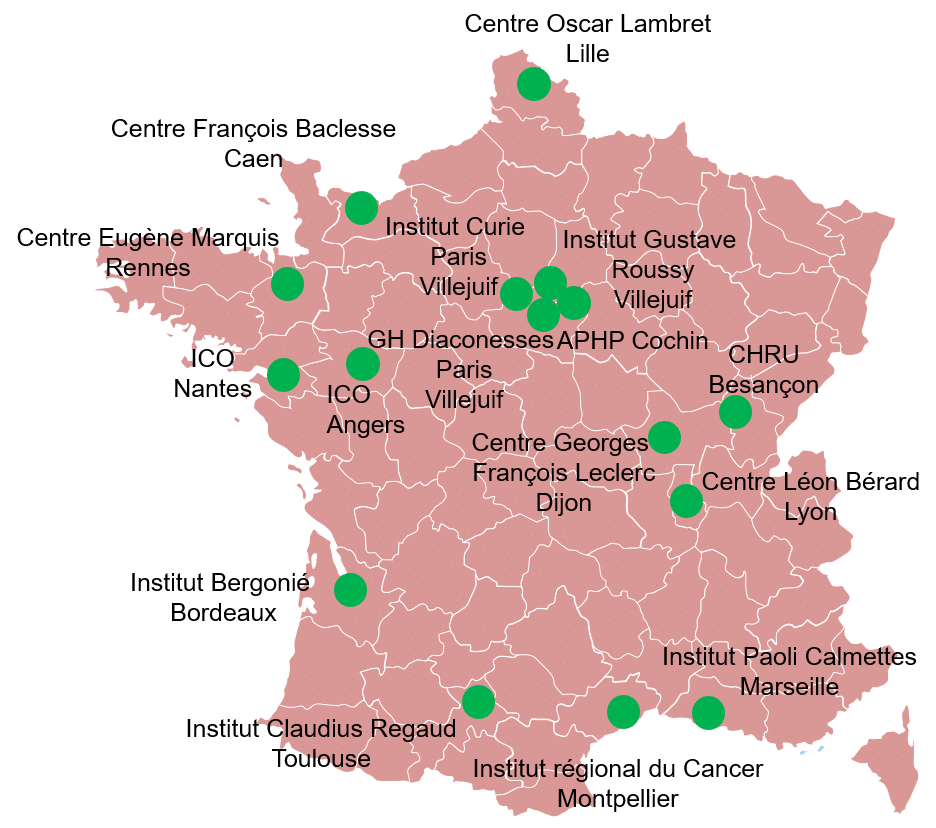
Depuis le début du projet, et malgré la crise sanitaire liée à la COVID-19, 15 centres ont pu être ouverts et sont actifs à ce jour.